EVENTRACIÓN
DEL DIAFRAGMA
Prof. Dr.
Irfan Yalcinkaya
Universidad
de Ciencias de la Salud, Facultad de Medicina Hamidiye de Estambul,
Departamento de Cirugía Torácica, Centro de Investigación en Salud y
Aplicaciones de Enfermedades Torácicas y Cirugía Torácica Sureyyapasa, Clínica
de Cirugía Torácica
Correo
electrónico: profdrirfanyalcinkaya@gmail.com
Resumen: En pacientes sintomáticos con
eventración diafragmática, la plicatura mínimamente invasiva es la principal
opción.
Palabras clave: Eventración diafragmática,
Plicatura, Cirugía toracoscópica videoasistida, Cirugía mínimamente invasiva
Definición,
historia y etiología
La
eventración diafragmática es la elevación permanente de toda o parte de la
lámina diafragmática, siempre que no se alteren las partes costales ni las
conexiones orgánicas. Otra definición es la elevación permanente del
hemidiafragma sin defecto en las inserciones musculares del diafragma ni
alteración de la integridad entre las cavidades pleural y peritoneal. Los
términos eventración y parálisis suelen confundirse. La parálisis describe la
degeneración muscular resultante de la denervación y es una de las patologías
que inician la eventración. Sin embargo, la eventración no siempre se acompaña
de parálisis. A pesar de ello, el término eventración se utiliza
simultáneamente para describir tanto la parálisis como la eventración del
diafragma. De hecho, cualquier tipo de elevación del diafragma, ya sea
eventración, parálisis o cualquier otra causa etiológica, se denomina elevación
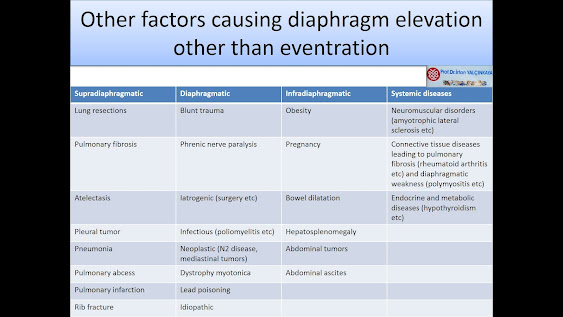
del diafragma. (Tabla 1)
Tabla
1. Otros factores que causan elevación del diafragma (elevación) además de la
eventración
La
elevación diafragmática fue descrita y publicada por primera vez por Jean Louis
Petit en 1760. El término "eventración diafragmática" fue utilizado
por primera vez por Beclard en 1829.
Si
bien es imposible identificar la etiología en la mayoría de los pacientes
(eventración diafragmática idiopática), las neoplasias malignas, los
traumatismos, las infecciones, las causas iatrogénicas (cirugía mediastínica y
cardíaca) y las enfermedades neuromusculares son factores etiológicos
importantes. Si bien la causa no siempre se explica por completo, la
eventración diafragmática congénita y adquirida se divide en dos categorías:
las relacionadas con la parálisis del nervio frénico y las que no. Es una de
las patologías poco frecuentes que a menudo se detecta incidentalmente tras un
traumatismo o durante las investigaciones sobre la etiología de la disnea.1
Si bien la causa puede identificarse en muchos pacientes, en algunos permanece
incierta. Se cree que las infecciones virales son la causa subyacente en estos
pacientes.2
La
causa principal de la eventración diafragmática congénita es un defecto
congénito del desarrollo de la porción muscular del diafragma, caracterizado
por una disminución del número de fibras musculares. La eventración
diafragmática adquirida se puede dividir en dos categorías: paralítica y no
paralítica. La causa principal de la eventración diafragmática paralítica es la
disfunción del nervio frénico tras un traumatismo, un tumor o una cirugía. En
casos de lesión del nervio frénico, la eventración diafragmática se observa en
el lado afectado.
Diagnóstico
La
eventración diafragmática, aunque poco frecuente, es más común en hombres y
generalmente predomina en el lado izquierdo. El síntoma más común de la
eventración diafragmática adquirida en adultos son los problemas respiratorios.
Dado que el diafragma es el principal músculo respiratorio, la mayoría de los
pacientes se quejan de aumento de la disnea, especialmente con el esfuerzo y en
decúbito supino. Con menor frecuencia, también puede presentarse tos, dolor
retroesternal o epigástrico. La insuficiencia respiratoria también puede
deberse a una enfermedad pulmonar subyacente o a una reserva pulmonar reducida.
Náuseas, vómitos, gases y distensión abdominal, eructos o un aumento anormal de
los ruidos intestinales también pueden presentarse como síntomas. También puede
asociarse con trastornos del sueño. Por lo tanto, se debe realizar una
polisomnografía en pacientes con eventración/parálisis diafragmática que
presenten síntomas y también presenten trastornos del sueño. Los pacientes con
diagnóstico de síndrome de apnea obstructiva del sueño pueden beneficiarse de
la cirugía, ya que los síntomas suelen mejorar o aliviarse. Esto también puede
ayudar a prevenir las comorbilidades a largo plazo de los trastornos del sueño.3,4
El
diagnóstico suele realizarse incidentalmente mediante radiografía de tórax
posteroanterior (PA) o lateral. Si bien la elevación del diafragma en la
radiografía directa puede no indicar parálisis diafragmática, esta puede
descartarse si no se observa una elevación del diafragma. La tomografía
computarizada (TC) torácica y, cuando es necesaria, la ecografía también son
métodos valiosos para mostrar la patología subyacente. (Figura 1) Sin embargo,
la capacidad de estos métodos para distinguir la eventración diafragmática de
las hernias es limitada. La resonancia magnética también puede utilizarse
cuando sea necesario.
Figura
1: Eventración diafragmática izquierda (radiografía de tórax PA, radiografía de
tórax lateral izquierda), Eventración diafragmática izquierda en la TC
torácica.
Si
el nervio frénico está afectado, los movimientos del diafragma se reducen o
desaparecen en la fluoroscopia, o se pueden observar movimientos paradójicos
del diafragma. En pacientes que se inspiran repentinamente durante la
fluoroscopia, el diafragma normal se mueve hacia abajo, mientras que el
diafragma paralizado se mueve hacia arriba. Definitivamente, se debe realizar
una fluoroscopia o una ecografía, especialmente en casos con eventración del
diafragma derecho. Hoy en día, la fluoroscopia ha dado paso casi por completo a
la ecografía. El grosor del diafragma se puede medir fácilmente y los
movimientos del diafragma se pueden evaluar con la ecografía torácica. No se
debe olvidar que las patologías debajo del diafragma (como la hepatomegalia, el
absceso subfrénico, las patologías intraabdominales) pueden causar una
elevación del diafragma derecho, y el derrame pleural y los quistes pericárdicos
también pueden simular una eventración del diafragma.
Las
pruebas de función pulmonar (PFP) pueden ser útiles en la evaluación de
pacientes disneicos con eventración diafragmática, quienes a menudo presentan
valores disminuidos de FEV1 y FVC. Dado que el diafragma disfuncional no puede
retraerse lo suficiente, se observa una disminución de los volúmenes pulmonares
y la compliancia. Esto se refleja en los valores espirométricos, y los valores
de FVC y FEV1 están disminuidos. Aunque los valores de las PFP suelen ser
anormales en pacientes sintomáticos con eventración/parálisis diafragmática,
estos valores a menudo no se relacionan con la gravedad de la disnea. Las PFP
son el criterio más objetivo utilizado para excluir otros factores en el
diagnóstico diferencial de la disnea, en la evaluación preoperatoria en la
eventración, en el seguimiento posoperatorio y en la respuesta a la cirugía.
En
el diagnóstico diferencial, se deben evaluar cuidadosamente los factores que
causan o exacerban la disnea de esfuerzo, como la enfermedad pulmonar
obstructiva crónica, la insuficiencia cardíaca congestiva y la obesidad
mórbida.
Tratamiento
En
presencia de eventración y parálisis diafragmática sintomática, el tratamiento
es quirúrgico. Independientemente de la etiología, la plicatura es el principal
método quirúrgico.2,5
El
objetivo de la plicatura quirúrgica es estabilizar el diafragma atrófico,
delgado, flácido y elevado para evitar el desplazamiento de los órganos
abdominales hacia el lado eventrador durante la inspiración y prevenir la
atelectasia lineal parenquimatosa resultante del desplazamiento y la compresión
del mediastino por el diafragma elevado. Además, al reducir la elevación
diafragmática a su posición normal mediante la plicatura, se restablece la presión
negativa intratorácica necesaria para la expansión pulmonar contralateral,
mejorando así el rendimiento físico.2,6
En
casos asintomáticos y en la eventración secundaria causada por neoplasias,
incluso si se detecta eventración en la radiografía de tórax, la cirugía no
está indicada a menos que sea sintomática y necesaria. (Figura 2)
Figura
2. Caso sin indicación quirúrgica.
La
cirugía está indicada cuando los síntomas respiratorios (generalmente disnea,
especialmente disnea de esfuerzo u ortopnea, con menos frecuencia tos) o cuando
los hallazgos gastrointestinales (dispepsia, meteorismo) están a un nivel que
afectará la vida del paciente. Una vez excluida la neoplasia, se puede decidir
la cirugía considerando la gravedad clínica del paciente y la duración de los
síntomas. Si la causa de la eventración es la parálisis y los síntomas son
nuevos, se puede esperar de 6 a 12 meses para que el cuadro se aclare en estos
pacientes, y en casos distintos a la parálisis, creemos que no es necesario
esperar para la cirugía en pacientes con síntomas clínicos (disnea de esfuerzo)
y eventración demostrada radiológicamente. La resolución espontánea es posible,
aunque rara vez, en eventraciones que ocurren en el período postoperatorio
temprano. Los casos asintomáticos deben ser monitoreados y se debe considerar
el tratamiento quirúrgico en caso de síntomas o deterioro de las funciones
respiratorias. Además, cuando se produce una lesión del nervio frénico en
pacientes sometidos a cirugía torácica (especialmente en neumonectomía), se
puede realizar una plicatura profiláctica del diafragma en la misma sesión para
reducir futuras complicaciones respiratorias.7 En el caso de los
pacientes con asistencia respiratoria, la plicatura no está contraindicada si
está indicada.
En
1916, Wood propuso por primera vez la idea de que arrugar el diafragma podía
reducir su tamaño. En 1923, Morrison realizó la primera cirugía de eventración
exitosa y definió el principio quirúrgico que aún se utiliza.
A
lo largo de la historia se han descrito y utilizado numerosos métodos en la
cirugía de eventración diafragmática. El método tradicional para pacientes con
eventración diafragmática sintomática es la plicatura abierta transtorácica o
transabdominal. Este método puede proporcionar un alivio significativo de los
síntomas y una mejora significativa de la función respiratoria. Sin embargo, la
cirugía abierta es invasiva y conlleva cierta morbilidad e incluso mortalidad.
No es una buena opción, especialmente para pacientes con múltiples comorbilidades
y baja capacidad pulmonar. Además, a pesar de la pequeña incisión utilizada en
esta cirugía, diseñada para reducir y aliviar la dificultad respiratoria, puede
causar dolor y restricción de la función respiratoria en el postoperatorio, lo
que reduce el pronóstico esperado.²
Para
minimizar las desventajas de la cirugía transtorácica abierta, en 1995,
Gharagozloo et al. realizaron la primera plicatura diafragmática toracoscópica
en un paciente de 72 años con afectación del nervio frénico izquierdo y
parálisis diafragmática izquierda debido a un carcinoma tímico. Este
procedimiento, salvo por el uso de asistencia por video, es técnicamente
idéntico al abordaje transtorácico clásico. En 1996, Mouroux et al.
desarrollaron y publicaron un método toracoscópico técnicamente más aplicable
que el método de Gharagozloo.8
Las
primeras aplicaciones de la VATS se realizaron principalmente en lactantes y
niños.9 En la literatura, las primeras series de publicaciones en adultos
suelen incluir casos de toracotomía y VATS. Hoy en día, los métodos quirúrgicos
abiertos han sido reemplazados por métodos quirúrgicos mínimamente invasivos.
La cirugía abierta se prefiere solo en pacientes en quienes la intubación con
un tubo de doble luz para VATS no es factible, el paciente no la tolera o no
puede realizarse una cirugía mínimamente invasiva debido a adherencias
pleurales/peritoneales graves debido a enfermedades o cirugías previas. (Tabla
2)
Tabla 2.
Métodos quirúrgicos para patologías diafragmáticas
En
el abordaje VATS, el paciente se coloca en decúbito lateral y 30 grados de
Trendelenburg invertido, como en la cirugía abierta. El primer puerto se abre
desde el sexto espacio intercostal (ACI) en la línea axilar media y la
ubicación de los otros 2 puertos se determina después de la exploración del
diafragma, y algunos cirujanos utilizan CO2 para deprimir el
diafragma. Durante la cirugía, la plicatura se realiza utilizando solo
instrumentos toracoscópicos (Endograsper, Endostitch, etc.). En la literatura,
el número de puertos utilizados para VATS varía entre 2 y 4, y se afirma que
este procedimiento se puede realizar con un solo puerto. 10 Aunque los
instrumentos endoscópicos utilizados en el procedimiento VATS son adecuados
para la eventración del diafragma en bebés y niños, es relativamente más
difícil realizar una plicatura con suficiente tensión con instrumentos
endoscópicos en adultos porque el diafragma tiene una mayor superficie y un
mayor grosor.
En
la plicatura diafragmática con RATS, el paciente se coloca en decúbito lateral,
con la cabeza en Trendelenburg invertido de 10 grados. El primer puerto se crea
desde el punto donde se considera que el diafragma está más alto y se inyecta
CO₂ en la cavidad intratorácica. A continuación, se abre el puerto de la cámara
desde la cuarta arteria carótida interna (ACI) y, tras la exploración, se abren
dos puertos más para los brazos robóticos y se aplica la plicatura. Si bien la
imagen tridimensional y la ausencia de restricción de movimiento durante la
plicatura parecen ser algunas de las ventajas, el alto coste de la RATS y su
difícil acceso y difusión pueden considerarse entre las desventajas de este
método.
Otro
método es el híbrido, denominado minitoracotomía videoasistida. Este método
implica una plicatura mediante un puerto de cámara y una toracotomía de
utilidad. Esto permite el uso práctico de instrumental quirúrgico abierto, y el
procedimiento se puede realizar con la misma facilidad que la cirugía abierta.
El espacio intratorácico se puede iluminar y, al sujetar y traccionar el diafragma,
las estructuras subdiafragmáticas se pueden visualizar fácilmente mediante
transiluminación. Suturar el diafragma con un grosor y una longitud suficientes
es difícil con una endodoncia, lo que dificulta lograr una tensión adecuada.
Además, los 3-4 puertos utilizados en la VATS permiten lograr una incisión de
utilidad total. Este método, descrito inicialmente por Lai y Paterson en 1999 y
reportado como un solo caso, fue modificado posteriormente por Rombolá et al. y
aplicado en 18 casos.10.11
Hemos
aplicado con éxito una versión modificada de estos dos métodos con
características diferentes en casos con eventración diafragmática.12-16
En
este método, el paciente fue intubado bajo anestesia general con un tubo de
intubación de doble luz según el lado. Los pacientes fueron acostados en la
mesa de operaciones en posición de decúbito lateral con el lado de la operación
hacia arriba, con la cabeza 30-45 grados más alta. De esta manera, los órganos
abdominales fueron bajados y la presión de los órganos abdominales en el
diafragma fue reducida. El brazo en el lado de la operación fue posicionado de
una manera que no obstaculizara el movimiento de la endocámara. Se insertó una
sonda nasogástrica para proporcionar descompresión gástrica y reducir la
distensión abdominal. Este procedimiento es especialmente importante en el lado
izquierdo, permitiendo así que el diafragma descienda más fácilmente y
reduciendo la tensión, permitiendo una maniobrabilidad más fácil para el
cirujano. Puede que no se realice en el lado derecho, pero sí se puede. En
estos pacientes, no es necesaria una limpieza intestinal adicional.
El
cirujano que realiza la cirugía se coloca detrás del paciente si la eventración
está en el lado derecho y delante del paciente si la eventración está en el
izquierdo. Primero, se creó un puerto de 10 mm (5 mm) para la endocámara en la
3.ª o 4.ª ACI en la línea axilar. Utilizando una lente óptica de cero grados
(30 grados), se evaluaron la cavidad torácica y el diafragma eventrado. Se
inició la ventilación unilateral y se desinfló el pulmón del lado que se iba a
plicar. Se identificó la unión del diafragma adelgazado y eventrado a la pared
torácica y se realizó una toracotomía utilitaria de 3-4 cm en la línea axilar
media, dos costillas por encima (normalmente la 7.ª u 8.ª ACI). Esto determinó
el nivel de tensión del diafragma (se podía usar una aguja de jeringa
transtorácica si era necesario) y proporcionó el espacio adecuado para trabajar
con el instrumental utilizado en cirugía abierta (o, preferiblemente, con
instrumental abierto desarrollado para toracoscopia). En la retracción de
toracotomía utilitaria, inicialmente se utilizaron retractores pediátricos y
retractores de Weitlaner, y posteriormente, en todos los casos, se utilizaron
retractores de protección de heridas (Alexis, etc.).
Utilizando
un portaagujas y pinzas, las suturas se colocaron primero a lo largo de la
línea media del diafragma, comenzando desde el punto más cercano a la inserción
del diafragma a la pared torácica y extendiéndose hasta el punto de inserción
del pericardio, utilizando una sola fila continua de sutura de seda del n.º 1
anudada con aguja. Las suturas iniciales se pueden colocar directamente
observando visualmente el diafragma a través del retractor y aplicando un
cabestrillo con las suturas. Las suturas finales se pueden colocar fácilmente
observando el diafragma en un monitor. El diafragma se levantó con pinzas o una
pinza, y la plicatura se realizó mediante transiluminación con la luz de una
cámara, evitando dañar los órganos abdominales. Cuando la plicatura era más
medial, la línea de plicatura se tensó con un dedo en ambos extremos de la
sutura y se hizo un nudo cerca de la toracotomía utilitaria. Se utilizó un
empujador de nudos si fue necesario. Esta primera fila de suturas resaltó las
demás líneas de plicatura, simplificando los procedimientos posteriores. Luego,
de la misma manera, se colocaron dos filas de puntadas a ambos lados de esta
primera fila de puntadas para proporcionar suficiente tensión en el diafragma,
y se bajó el diafragma a su posición normal.
Si
el diafragma del paciente es extremadamente delgado y se sospecha que las
suturas pueden desgarrarse, se puede utilizar una sutura con compresa. Durante
la plicatura, se tuvo cuidado de no intentar pasar la aguja a través de los
pliegues formados cuando el diafragma, que está suelto y laxo, se sujetó con
pinzas y de no insertar la aguja ni superficial ni demasiado profundamente. De
esta manera, el diafragma se pliega con mucha fuerza y se previene una
posible complicación relacionada con las estructuras debajo del diafragma.
Después de verificar la tensión del diafragma con un dedo o una herramienta, se
revisó todo el campo con la ayuda de una cámara. Se debe tener cuidado de no
sobretensionar el diafragma como resultado de la plicatura, ya que las suturas
colocadas pueden desgarrarse en casos en que aumenta la presión intraabdominal.
Se
insertó un tubo pleural de calibre 24 o 28 en el espacio pleural a través de
una toracotomía utilitaria y se colocó en la cavidad pleural con su punta en el
ápice. La incisión debe cerrarse muy bien; de lo contrario, puede producirse
una hernia pulmonar, y creo que se puede colocar una sutura intercostal única
si se considera necesario. Se tomaron radiografías de tórax PA postoperatorias
a todos los pacientes para ver los niveles del diafragma en el período inicial.
La sonda nasogástrica se terminó con el inicio de las deposiciones en el primer
día postoperatorio y todos los pacientes comenzaron con una dieta blanda. Si no
hay drenaje ni fuga de aire y el pulmón está expandido en la radiografía de
tórax PA, el drenaje generalmente se puede retirar al final del primer o
segundo día postoperatorio. El paciente al que se le haya retirado el drenaje
puede ser dado de alta después de una radiografía de tórax de control. Después
del alta, se le aconseja al paciente que no esté estreñido por un tiempo y que
no levante objetos pesados.
En
la literatura se describen muchos métodos para la plicatura del diafragma:
suturas en U atadas a mano, suturas de matriz, suturas continuas con o sin
compresas o grapas, métodos con o sin malla, resección de una porción del
diafragma y unión de la porción restante de extremo a extremo con suturas
superpuestas.8,14
Aunque
no existe ningún estudio que compare la VATS con los métodos de plicatura, un
estudio de Evman et al. comparó las técnicas de plicatura realizadas mediante
toracotomía. En una serie de 42 casos, se compararon las técnicas de plicatura
en acordeón y laparoscópica, y se observó un aumento similar en los valores
espirométricos entre ambos grupos. Se destacó un aumento en las pruebas
espirométricas independientemente de la técnica.17 La elección del
método de plicatura depende de la experiencia, la formación y las preferencias
del cirujano. La mejoría de la disnea es el indicador más importante del éxito
clínico.
Aplicamos
y preferimos la plicatura en acordeón con suturas continuas no absorbibles,
como la seda. Sin embargo, también se pueden utilizar suturas de prolene y
poliéster. También utilizamos suturas de compresa en algunos casos donde el
diafragma estaba extremadamente delgado y pensamos que se rompería con las
suturas. No preferimos las grapas debido a la preocupación de que estas se
rompan debido a la tensión creada en el diafragma, ni la resección del
diafragma debido a la necesidad de tejido suficientemente grueso, incluso si
está delgado. No recomendamos la malla y creemos que solo se puede utilizar en
casos recurrentes.
En
casos de eventración diafragmática derecha, se requiere extrema precaución y
meticulosidad. Se debe investigar a fondo la causa de la eventración y, si es
posible, realizar una fluoroscopia. La fluoroscopia ya no se utiliza con
frecuencia, y en los últimos años se ha optado por la ecografía diafragmática.
Esta permite medir fácilmente el movimiento y el grosor del diafragma. Se deben
evaluar cuidadosamente los síntomas y la función respiratoria del paciente para
detectar EPOC, obesidad e insuficiencia cardíaca. En cuatro casos de
eventración diafragmática derecha, no se indicó cirugía, mientras que en dos
casos, el diafragma se encontró normal durante la cirugía y se abandonó la
plicatura.
Incluso
en casos con antecedentes de traumatismo, es posible encontrar eventración en
lugar de rotura del diafragma durante una toracotomía. Además, se pueden
detectar otras patologías como hernia diafragmática y quistes pericárdicos. Por
lo tanto, recomendamos iniciar la VATS en todas las patologías diafragmáticas,
incluso si hay antecedentes de traumatismo. Si bien la cirugía cerrada se puede
convertir en cirugía abierta en cualquier momento, la conversión a cirugía
cerrada no es posible.
En
la Clínica de Cirugía Torácica de la Universidad de Ciencias de la Salud,
Centro de Investigación y Aplicación de la Salud en Enfermedades Torácicas y
Cirugía Torácica Sureyyapasa de Estambul, entre diciembre de 2009 y mayo de
2025, 106 casos con síntomas de disnea de esfuerzo y diagnóstico de parálisis y
eventración diafragmática se sometieron a cirugía mínimamente invasiva con
plicatura diafragmática. En todos los casos, las molestias clínicas mejoraron
total o sustancialmente en el postoperatorio. No se observó mortalidad, y más
de diez casos presentaron complicaciones mínimas (hernia pulmonar en un caso) y
un caso presentó recurrencia, con un seguimiento adecuado. (Figura 3)
Figura
3. Nuestro caso número 106 sometido a plicatura VATS
En
el estudio de tesis doctoral de 50 casos titulado “El efecto de la cirugía
mínimamente invasiva en las funciones respiratorias en la eventración
diafragmática” realizado en 2017 por el Dr. Deniz Gürer y para el cual fui
asesor de tesis en la misma institución; cuando se compararon los valores
preoperatorios y postoperatorios de FEV1 (% y lt) de los pacientes, se encontró
un aumento estadísticamente significativo en ambos parámetros (p<0,001).
Hubo un aumento promedio de 12,1% en los valores de FEV1 (lt). De manera
similar, cuando se compararon los valores preoperatorios y postoperatorios de
FVC (% y lt), se encontró un aumento estadísticamente significativo en ambos
parámetros (p<0,001). Hubo un aumento postoperatorio de 11,5% en los valores
de FVC (lt). Se detectó recurrencia en un paciente durante los seguimientos a
largo plazo; este paciente no aceptó la cirugía y fue seguido.
La
cirugía está indicada en casos sintomáticos con eventración diafragmática y
disnea de esfuerzo, especialmente en el lado izquierdo. Actualmente, la
plicatura diafragmática mínimamente invasiva es un método sencillo, rápido y
altamente efectivo para las patologías diafragmáticas, en particular aquellas
que afectan otras estructuras torácicas, y en particular para la eventración
diafragmática. Este método quirúrgico, que utiliza el mismo instrumental
empleado en la cirugía abierta, logra una tensión diafragmática adecuada y
proporciona mejoras estadísticamente significativas en las pruebas
espirométricas. Además, al igual que con otros procedimientos mínimamente invasivos,
se reduce el dolor y la morbilidad postoperatorios, se aumenta la comodidad del
paciente y se acelera la recuperación, lo que resulta en un alta más rápida.18-21
Reiteramos
que la plicatura mínimamente invasiva es la opción principal para pacientes
sintomáticos con eventración diafragmática.
*Visualización
recomendada: Cirugía mínimamente invasiva para eventración diafragmática, https://www.youtube.com/watch?v=GKqM4OX37Xs
*Visualización
recomendada: Prof. Dr. İrfan Yalçınkaya, Cirugía mínimamente invasiva para
eventración y parálisis diafragmática, Facultad de Cirugía Torácica, 2024,
https://www.youtube.com/watch?v=3DOxq0VrRRU&t=245s
Fuentes:
1. Yalçınkaya İ. Dispne
etyolojisinin araştırılması sırasında saptanan nadir bir patoloji: Diyafram
evantrasyonu (Una patología rara detectada durante la investigación de la
etiología de la disnea: eventración del diafragma). Akciğer Bülteni
2019;5(2):51-5.
2. Yalçınkaya İ. Diyafram paralizisi ve evantrasyonu
(Parálisis del diafragma y eventración). Yalçınkaya İ, editör. Diyafram
Hastalıkları. Toraks Cerrahisi Bülteni 2013;4(4):266-71.
3. Oruc O, Sarac S, Afsar GC, Topcuoglu OB,
Kanbur S, Yalcinkaya I, Tepetam FM, Kirbas G. Is
polysomnographic examination necessary for subjects with diaphragm pathologies? Clinics 2016;71(9):506-10.
4.
Sarac S, Salturk C,
Oruc O, Kanbur Metin S, Bayram S, Karakurt Z, Yalcınkaya
I. Sleep-related breathing disorders in diaphragmatic pathologies. Sleep
and Breathing 2021;26:959-963.
5.
Derdiyok
O, Yalçınkaya İ. Diyafram patolojilerinde cerrahi yaklaşım (Abordaje
quirúrgico de las patologías del diafragma). In: Göğüs Cerrahisi. Metin M,
Cansever L, Sezen CB (eds). Akademisyen Yayınevi, Ankara, 2022, Sh.415-20.
6. Işık AF, Yalçınkaya İ, Kurnaz M. Erişkinlerde
diyafragma yükselmeleri; Cerrahi gerekli mi? (Elevaciones diafragmáticas en
adultos; Es necesaria cirugía?) Van Medical Journal 2002;9(1):33–7.
7. Yalçınkaya
İ, Doğruyol MT. Prophylactic chest surgery procedures. In: Dilek ON, Uranues
S, Latifi R, eds. Prophylactic Surgery.
1 st ed. Switzerland: Springer; 2021. p. 371-8.
8. Gürer D, Atinkaya C, Yalçınkaya İ. Diyafram
eventrasyonu (Eventración del diafragma). In: Eren TŞ, editor. Torasik Cerrahi.
1st ed. İstanbul: İstanbul Tıp Kitapevi 2019; p. 53–60.
9. İrdem AK, Doyurgan O, Kılıç Y, Balık H.
İnfantlarda konjenital kalp cerrahisi sonrasında gelişen diyafram felcinin
cerrahi tedavisi (Tratamiento quirúrgico de la parálisis diafragmática que se
desarrolla después de una cirugía cardíaca congénita en bebés.). Dicle Tıp Dergisi 2024;51(3):415-24.
10. Rombolá C, Crespo MG, López PT, Martínez AH, Atance
PL, Ramírez AT, et al. Video-assisted minithoracotomy diaphragmatic plication:
respiratory effects in adults. Thorac Cardiovasc Surg. 2016;64(08):647–53.
11. Lai DTM, Paterson HS. Mini-thoracotomy for
diaphragmatic plication with thoracoscopic assistance. Ann Thorac Surg. 1999;68(6):2364–5.
12. Yalçınkaya İ. Plikasyon (Plegamiento). In: Toker A,
Batırel HF, editors. Çağdaş Videotorakoskopik Cerrahide Teknikler ve Sonuçlar.
1st ed. İstanbul: Nobel Tıp Kitabevi; 2014; p. 157–62.
13. Yalcinkaya I, Evman S, Lacin T, Alpay L, Kupeli M, Ocakcioglu
I. Video-assisted minimally invasive diaphragmatic plication: feasibility of a
recognized procedure through an uncharacteristic hybrid approach. Surg Endosc.
2017;31(4):1772–7.
14. Yalçınkaya İ, Atinkaya Baytemir C. Diyafram
Eventrasyonu ve Paralizisi. In: Yalçınkaya İ, editor. Diyafram Hastalıkları.
1st ed. Ankara: Türkiye Klinikleri Yayınevi, 2020; p. 38–44.
15.
Doğruyol
MT, Yalçınkaya İ. Chapter 75: VATS plication of diaphragm. In: Advanced
Thoracic Surgery; Balcı AE, Ersöz H, Yüksel M (editors), Ankara; Akademisyen
Kitabevi, 2021;781-5.
16. Yalçınkaya
İ. VATS ile diyafram cerrahisi (Cirugía de diafragma con VATS). In: Minimal
İnvazif Torasik Yaklaşımlar; Metin M, Sezen CB (editors), İstanbul; Medical
Network, 2021;291-308.
17. Evman S, Tezel C,
Vayvada M, Kanbur S, Urek S, Baysungur V, Yalçınkaya I. Comparison of mid-term
clinical outcomes of different surgical approaches in symptomatic diaphragmatic
eventration. Ann Thorac Cardiovasc Surg. 2016;224-29.
18. Nardini
M, Jayakumar S, Migliore M, Nosotti M, Paul I, Dunning J. Minimally invasive
plication of the diaphragm: A single-center prospective study. Innovations 2021;16(4):343-9.
19. Gritsiuta
AI, Gordon M, Bakhos CT, Abbas AE, Petrov RV. Minimally invasive diaphragm
plication for acquired unilateral diaphragm paralysis: A systematic
review. Innovations 2022;17(3):180-90.
20. Gilbert
A, Wei B. Diaphragmatic plication: current evidence and techniques in the
management of the elevated hemidiaphragm. Video-Assisted Thoracic Surgery 2023;8.
21. Balamurugan
G, Bhandarwar A, Wagh A, Bakhshi G, Ansari K, Bhondve S, Dhimole N, Jawale H.
Comparison of short-term outcomes of video-assisted thoracoscopic (VATS)
plication of diaphragmatic eventration-a six-year prospective cohort
study. Updates in Surgery 2024;76(1):279-88.
![PROF. DR. İRFAN YALÇINKAYA [GÖĞÜS CERRAHİSİ - THORACIC SURGERY]](https://blogger.googleusercontent.com/img/a/AVvXsEjOSqhx1rvc70zQbuI67m6C9chfm5r0YlXuv4DqpwwqdvsLZ8aOYvoGva_4n8-3wnrAY-3CNTngHJcd-Kb6E0r1XGpiBhgX3KpFh7bqVwFaUv74e00zz1QzKGA2aHfgKK7GP_l7of1mnPNrvWwnx9DL4G3Icb6QtvT4WMKWPaHB_bCIm0hE3Z8_Mc-7cMY=s752)









Hiç yorum yok:
Yorum Gönder